Sociedad
Se entregó el hijo del narcotraficante ‘El Chapo’ Guzmán

26 de julio de 2024
Ismael «El Mayo» Zambada, uno de los principales líderes del Cártel de Sinaloa (CDS), se entregó a las autoridades estadounidenses cerca de El Paso, Texas, junto a Joaquín Guzmán López, hijo de Joaquín «El Chapo» Guzmán, quien cumple cadena perpetua.
El Mayo Zambada, acusado de ser uno de los mayores traficantes de fentanilo, podría haberse entregado debido a su estado de salud, ya que un informe de la Administración de Control de Drogas (DEA) resalta que «Ismael Zambada García se encuentra enfermo».
El portal Border Report indicó que el líder del CDS fue detenido en el aeropuerto Doña Ana County International Jetport, en Santa Teresa, en la tarde de este jueves.
El Mayo Zambada está en el narcotráfico desde la década de 1980, y desde hace 40 años que aparece en los registros de inteligencia de Estados Unidos como la cabeza visible del CDS.
El CDS se consolidó al unirse a las familias de Joaquín «El Chapo» Guzmán y de Juan José «El Azul» Esparragoza Moreno, asesinado en 2014.
Zambada se había convertido en el principal objetivo de Estados Unidos, señalado como el principal productor, distribuidor, traficantes y vendedor de fentanilo en el pais, e incluso ofreció una recompensa de 15 millones de dólares.
También está acusado de dirigir una organización criminal, conspiración, homicidio y lavado de dinero.
Autoridades estadounidenses indicaron: «El Departamento de Justicia ha detenido a otros dos presuntos líderes del Cártel de Sinaloa, una de las organizaciones de narcotráfico más violentas y poderosas del mundo. Ismael Zambada García, o “El Mayo”, cofundador del Cártel, y Joaquín Guzmán López, hijo de su otro cofundador, fueron arrestados hoy en El Paso, Texas».
Joaquín Guzmán López, también buscado por la DEA, heredó los negocios criminales de su padre en el CDS. En 2015 participó en una operación para que se fugara El Chapo Guzmán del Penal del Altiplano.
País
Adorni negó censura al periodismo

El jefe de Gabinete, Manuel Adorni, negó esta mañana que el gobierno del presidente Javier Milei haya censurado a la prensa acreditada en la Casa Rosada con el cierre de la sala de periodistas por más de una semana.
Hoy se produjo la reapertura pero no se permitió el ingreso de Canal 13 y TN, canal que emitió imágenes del interior de la Casa Rosada sin autorización oficial.
Adorni se mantuvo en que se trató de un "hecho grave" y que las decisiones sobre la seguridad interna de la Casa de Gobierno las maneja Casa Militar.
Respecto de las polémicas en torno a la compra de inmuebles y sus viajes al exterior realizando gastos que no se condicen con su declaración jurada, insistió en que la causa se encuentra en la Justicia y que sólo dará explicaciones en tribunales.
Luego no precisó en qué fecha presentará su nueva declaración jurada aunque afirmó que lo hará "en tiempo y forma". Tiene plazo hasta el 31 de julio.
Asimismo, el jefe de Gabinete confirmó que volverá a un esquema de ruedas de prensa frecuentes. Si bien explicó que no las daría a diario, sí dio a entender que tendrán mucha regularidad.
Otra pregunta tuvo que ver con las encuestas que indican una caída en la imagen positiva del gobierno de Milei. El funcionario sostuvo que no gobiernan pensando en los sondeos de opinión sino en "mejorar la calidad de vida de los argentinos".
Tampoco habló sobre el aumento salarial de más de mil funcionarios nacionales que tuvieron los sueldos congelados hasta 2025. Entre enero y junio se estima que recibirán una suba del 123% para compensar el tiempo sin incrementos. Al respecto, Adorni dijo que no leyó las notas periodísticas y que tampoco haría declaraciones.
Sociedad
El Gobierno libera el mercado de vapeadores

El Gobierno nacional liberó el mercado de vapeadores y bolsas de nicotina creando un nuevo marco regulatorio que incluye la implementación de un registro obligatorio para fiscalizar la comercialización e importación.
El nuevo marco normativo para los productos de tabaco y nicotina de nueva generación fue aprobado por el Ministerio de Salud mediante la Resolución 549/2026, publicada este lunes en el Boletín Oficial.
Desde el Ejecutivo explicaron que “la medida tiene como objetivo reemplazar el esquema de prohibición vigente por un sistema de registro, control y fiscalización específico que permita establecer estándares mínimos de calidad y seguridad sanitaria para su comercialización”.
Asimismo, argumentaron que “la decisión se fundamenta en que la prohibición previa no logró impedir el acceso ni el consumo de estos productos”. Según datos recientes, los vapeadores y cigarrillos electrónicos registraron una prevalencia de consumo del 35,5% en adolescentes durante el último año, posicionándose entre las sustancias de mayor consumo en este grupo etario.
Frente a este escenario, la cartera sanitaria nacional avanzó en un modelo regulatorio alineado con experiencias internacionales implementadas en países como Estados Unidos y el Reino Unido.
Según lo establecido por la nueva resolución, los cigarrillos electrónicos, vapeadores, dispositivos de tabaco calentado, líquidos para vaporización y bolsas de nicotina son considerados productos elaborados con tabaco y deben cumplir con las disposiciones previstas en la Ley N° 26.687 y su normativa reglamentaria.
Esto implica la obligatoriedad de incorporar advertencias sanitarias en los envases, la prohibición de utilizar elementos de diseño que resulten atractivos para niños y adolescentes, imágenes de celebridades o mensajes engañosos, y restricciones específicas sobre aromas autorizados.
La norma, analizada por la Agencia Noticias Argentinas, también limita los sabores autorizados para su comercialización. Solo se permiten líquidos y sticks con sabor tabaco y bolsas de nicotina con sabor tabaco o mentol.
Asimismo, prohíbe expresamente los cigarrillos electrónicos desechables con soluciones precargadas, “considerados uno de los formatos de mayor atractivo para la iniciación juvenil”, según remarcaron desde Salud.
En este marco, también se creó el Registro Nacional de Productos de Tabaco y Nicotina (RNPTN) para “clasificar los productos según su tecnología y modalidad de uso, construir herramientas de monitoreo epidemiológico y ajustar las regulaciones en función de la evidencia científica disponible”.
Sobre este punto, desde la cartera que conduce Mario Lugones advirtieron que “aquellos productos que no se encuentren contemplados dentro de las categorías previstas no podrán ser importados ni comercializados en el país”.
La normativa también incorpora exigencias económicas y técnicas para productores e importadores. Las empresas deberán tramitar la inscripción de cada producto a través de la plataforma Trámites a Distancia (TAD), presentar declaraciones juradas, fórmulas completas, información toxicológica y certificados de análisis de emisiones emitidos por laboratorios acreditados.
Además, deberán informar datos vinculados a volumen de ventas y grupos etarios consumidores para fortalecer la vigilancia sanitaria y el monitoreo del acceso de menores. La inscripción tendrá una vigencia de cinco años y estará sujeta a renovación periódica, permitiendo al Estado reevaluar las condiciones de autorización de cada producto.
El Gobierno destacó la actualización normativa al señalar que “incorpora un modelo de regulación activa que fortalece la capacidad de fiscalización del Estado sobre productos cuyo consumo continúa expandiéndose, especialmente entre adolescentes y jóvenes”.
Además, resaltó que “a través de herramientas de registro, trazabilidad y vigilancia sanitaria, el Ministerio de Salud de la Nación busca reducir los riesgos asociados al consumo, prevenir el acceso de menores y combatir la comercialización ilegal de productos sin control sanitario”.
País
Donación de sangre: no más pedido de dadores de familiares
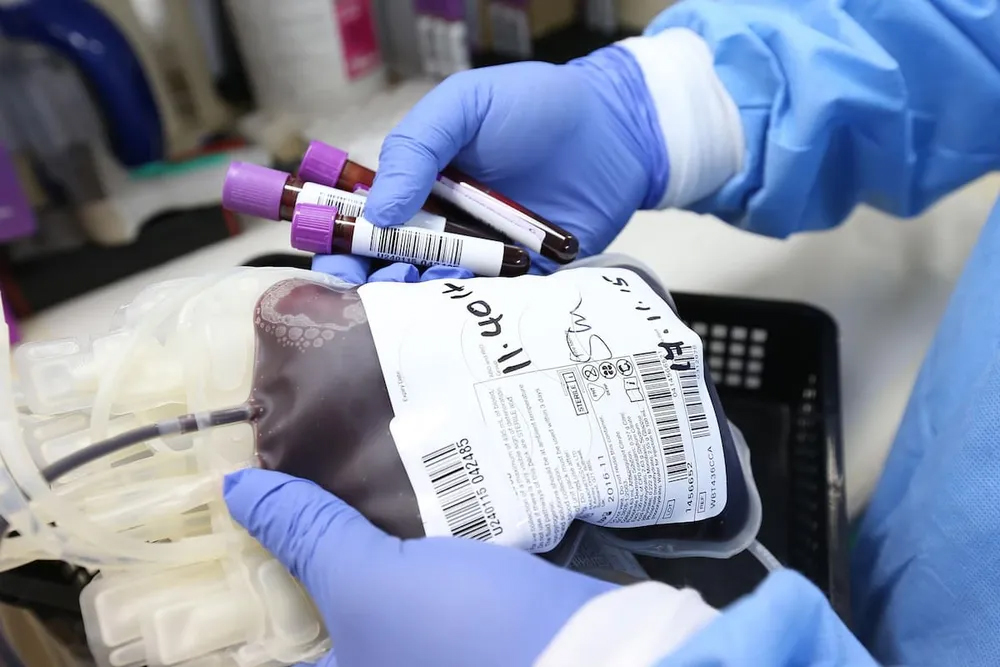
El Ministerio de Salud de la Nación actualizó las normas administrativas y técnicas que regulan el Sistema Nacional de Sangre. Luego de 10 años, la medida busca modernizar todo el proceso de donación y transfusión de sangre y el funcionamiento de los servicios de hemoterapia, inmunohematología y terapia celular del país para garantizar mayor seguridad tanto a los pacientes como a los donantes voluntarios.
Más noticias
Luján se pone más hermosa para festejar sus cuatro siglos.
Luján: premios millonarios para rediseñar el acceso a la Basílica
La Federación de Educadores Bonaerenses (FEB).
La FEB y Suteba, dos gremios docentes que van a las urnas para definir sus liderazgos
Los cambios fueron publicados en el Boletín Oficial, a través de la Resolución N° 536/2026, y la modificación más saliente es la referida al régimen de donación para paciente específico, es decir, los familiares no necesitarán impulsar colectas entre personas conocidas. Asimismo, la normativa actualiza los criterios de selección de donantes.
La resolución incorpora también nuevos lineamientos regulatorios para el procesamiento de terapias celulares así como de componentes especiales como el Plasma Rico en Plaquetas (PRP) y el Suero Autólogo Oftalmológico (SAO).
La medida entró en vigencia a partir de su publicación en el Boletín Oficial y las instituciones tendrán un plazo máximo de dos años para implementar los cambios tecnológicos y estructurales requeridos.
"La medida reemplaza el modelo de donación de reposición, vinculada a un paciente específico, por un modelo de donación 100% voluntaria y habitual. En este sentido, se prohíbe explícitamente condicionar la atención médica o las cirugías a la presentación de donantes por parte del paciente o sus familiares. Las donaciones destinadas a un paciente específico, solo se permitirán cuando exista una justificación terapéutica. De esta manera, se deja de trasladar la responsabilidad de conseguir sangre a los pacientes y familiares, y se garantiza mayor seguridad transfusional, dado que el donante voluntario y habitual presenta menor prevalencia de infecciones transmisibles", apuntó la cartera sanitaria en un comunicado.
Respecto a los criterios de selección de donantes, el nuevo marco normativo elimina la exclusión de grupos poblacionales enteros considerados de riesgo y propone evaluar solo las conductas del donante (como prácticas sexuales específicas o uso de drogas) y la evidencia científica. También se elimina el ayuno previo y se recomienda beber al menos 500 ml de agua o bebidas con sales media hora antes de la extracción.
De igual modo, en sintonía con los avances en las pruebas de tamizaje, se actualizan los tiempos de espera para donar según factores de riesgo. "Se difiere la donación por 6 meses para quienes hayan tenido una nueva pareja sexual o más de una pareja sexual en los últimos 3 meses y hayan tenido relaciones sexuales anales, hayan utilizado estrategias orales de profilaxis de preexposisión o postexposición, se haya realizado tatuajes, piercings o procedimientos estéticos invasivos, o hayan permanecido en instituciones penales por más de 72 horas", apuntó la nueva normativa.
Red integrada de sangre
Las modificaciones presentadas consolidan un modelo de red integrada de sangre, con procesos coordinados, trazabilidad y mayor capacidad de respuesta. Para ello, fortalece los Centros Regionales de Hemoterapia y dispone la desactivación progresiva de los Bancos de Sangre Intrahospitalarios para alcanzar mayores estándares de eficiencia, efectividad y seguridad transfusional. Establece también para todos los centros de hemoterapia, bancos de sangre y servicios de medicina transfusional del país, la obligatoriedad de informatizar los registros y garantizar sistemas de trazabilidad. Esto significa que cada proceso, desde la promoción de la donación voluntaria hasta que la sangre llega al paciente, deberá estar rigurosamente protocolizado, controlado y auditado.

